Gabapentinóide
Content

Gabapentinóides, também conhecidos como ligantes α2Δ, são uma classe de medicamentos que são derivados do neurotransmissor inibitório gama-aminobutírico (GABA) (isto é, análogos do GABA) que bloqueiam os canais de cálculo de tensão de subunidade α2Δ. Este local foi referido como o receptor de gabapentina (subunidade α2Δ), pois é o alvo dos medicamentos gabapentina e pregabalina.
Gabapentinóides clinicamente usados incluem gabapentina, pregabalina e mirogabalina, bem como um pró -fármaco de gabapentina, gabapentina enacarbil. Além disso, verificou -se que o fenão atua como gabapentinóide, além de sua ação de funcionar como agonista do receptor GABAB. Outros análogos como a imagabalina estão em ensaios clínicos, mas ainda não foram aprovados. Outros gabapentinóides que são usados em pesquisas científicas, mas não foram aprovadas para uso médico, incluem atagabalina, 4-metilpregabalina e PD-217,014. [Citação necessária]
Usos médicos
Gabapentinóides são aprovados para o tratamento da epilepsia, neuralgia pós -pó, dor neuropática associada à neuropatia diabética, fibromialgia, transtorno de ansiedade generalizada e síndrome das pernas inquietas. Alguns usos off label de gabapentinóides incluem o tratamento de insônia, enxaqueca, fobia social, transtorno do pânico, mania, transtorno bipolar e retirada de álcool. As evidências existentes sobre o uso de gabapentinóides na dor lombar crônica são limitadas e demonstram risco significativo de efeitos adversos, sem nenhum benefício demonstrado. Os principais efeitos colaterais incluem: uma sensação de sonolência e cansaço, pressão arterial diminuída, náusea, vômito e também alucinações visuais glaucomatosas, típicas para alucinógenos.
Efeitos colaterais
Farmacologia
Farmacodinâmica
Gabapentinóides são ligantes do local da subunidade α2Δ auxiliar de certos VDCCs e, assim, atuam como inibidores de VDCCs contendo subunidades α2Δ. Existem duas subunidades α2Δ de ligação a medicamentos, α2Δ-1 e α2Δ-2, e os gabapentinóides mostram afinidade semelhante por (e, portanto, falta de seletividade entre) esses dois locais. Os gabapentinóides são seletivos na ligação à subunidade α2Δ VDCC. No entanto, o fenão também se liga e atua como agonista do receptor de Gabab com menor afinidade (~ 5 a 10 vezes em um estudo). Apesar do fato de que a gabapentinóides são análogos do GABA, a gabapentina e a pregabalina não se ligam aos receptores GABA, não se convertem em agonistas do receptor GABA ou GABA in vivo e não modulam o transporte de GABA ou o metabolismo. Atualmente, não há evidências de que as ações relevantes da gabapentina e da pregabalina sejam mediadas por qualquer mecanismo que não seja a inibição de VDCCs contendo α2Δ. Embora gabapentinóides como a gabapentina, mas não a pregabalina, tenham sido encontrados para ativar os canais de potássio dependentes de tensão KV (KCNQ).
Os α-aminoácidos endógenos L-leucina e L-isoleucina, que se assemelham estreitamente com os gabapentinóides na estrutura química, são ligantes aparentes da subunidade α2Δ VDCC com afinidade semelhante à gabapentina e pregabalina (por exemplo, ic50 = 71 NM para L-isoleuckina) e estão presentes no líquido cefalorraquidiano humano em concentrações micromolares (por exemplo, 12,9 μM para L-leucina, 4,8 μM para L-isoleucina). Foi levantada a hipótese de que eles podem ser os ligantes endógenos da subunidade e que podem antagonizar competitivamente os efeitos dos gabapentinóides. De acordo, enquanto a gabapentina e a pregabalina têm afinidades nanomolares para a subunidade α2Δ, suas potências in vivo estão na faixa micromolar baixa, e a competição pela ligação por L-aminoácidos endógenos provavelmente é responsável por essa discrepância.
Em um estudo, os valores de afinidade (KI) dos gabapentinóides para a subunidade α2Δ expressos no cérebro de ratos foram de 0,05 μM para gabapentina, 23 μM para (r)-fenão, 39 μm para (s)-phenut e 156 μm para baclofeno. Suas afinidades (KI) para o receptor GABAB foram> 1 mm para gabapentina, 92 μM para (r)-fenão,> 1 mm para (s) fenão e 6 μM para baclofeno. Com base na baixa afinidade do baclofeno para a subunidade α2Δ em relação ao GABAB (diferença de 26 vezes), é improvável que sua afinidade pela subunidade α2Δ seja de importância farmacológica.
A pregabalina demonstrou potência significativamente maior (cerca de 2,5 vezes) do que a gabapentina em estudos clínicos.
Farmacocinética
AbsorptionGabapentina e pregabalina são absorvidas do intestino por um processo de transporte ativo mediado pelo grande transportador de aminoácidos neutros 1 (Lat1, SLC7A5), um transportador para aminoácidos como L-leucina e L-fenilalanina. Sabe -se que muito poucos (menos de 10 medicamentos) são transportados por este transportador. Ao contrário da gabapentina, transportada apenas pelo LAT1, a pregabalina parece ser transportada não apenas pelo LAT1, mas também por outras transportadoras. O LAT1 é facilmente saturável, portanto, a farmacocinética da gabapentina depende da dose, com biodisponibilidade diminuída e níveis de pico atrasados em doses mais altas. Por outro lado, esse não é o caso da pregabalina, que mostra farmacocinética linear e nenhuma saturação da absorção. Da mesma forma, a gabapentina Enacarbil é transportada não pelo LAT1, mas pelo transportador de monocarboxilato 1 (MCT1) e pelo transportador multivitamínico dependente de sódio (SMVT), e nenhuma saturação de biodisponibilidade foi observada com a droga até uma dose de 2,800 Mg. Da mesma forma que a gabapentina e a pregabalina, o baclofeno, um análogo próximo do fenão (o baclofeno especificamente o 4-clorofenão), é transportado pelo LAT1, embora seja um substrato relativamente fraco para o transportador.
A biodisponibilidade oral da gabapentina é de aproximadamente 80% a 100 mg administrada três vezes ao dia uma vez a cada 8 horas, mas diminui para 60% a 300 mg, 47% a 400 mg, 34% a 800 mg, 33% a 1.200 mg e 27 % a 1.600 mg, todos com o mesmo cronograma de dosagem. Por outro lado, a biodisponibilidade oral da pregabalina é maior ou igual a 90% e além de toda a sua faixa de dose clínica (75 a 900 mg/dia). Os alimentos não influenciam significativamente a biodisponibilidade oral da pregabalina. Por outro lado, os alimentos aumentam os níveis de gabapentina na área sub-curva em cerca de 10%. Os medicamentos que aumentam o tempo de trânsito da gabapentina no intestino delgado podem aumentar sua biodisponibilidade oral; Quando a gabapentina foi co-administrada com morfina oral (que diminui o peristaltismo intestinal), a biodisponibilidade oral de uma dose de gabapentina de 600 mg aumentou 50%. A biodisponibilidade oral da gabapentina enacarbil (como gabapentina) é maior ou igual a 68%, em todas as doses avaliadas (até 2.800 mg), com média de aproximadamente 75%. Em contraste com os outros gabapentinóides, a farmacocinética do fenão foi pouco estudada e sua biodisponibilidade oral é desconhecida. No entanto, parece ser pelo menos 63% em uma dose única de 250 mg, com base no fato de que essa fração de fenão foi recuperada da urina inalterada em voluntários saudáveis administrados essa dose.
A gabapentina em uma dose baixa de 100 mg tem um TMAX (tempo a pico de pico) de aproximadamente 1,7 horas, enquanto o TMAX aumenta para 3 a 4 horas em doses mais altas. O TMAX da pregabalina é geralmente menor ou igual a 1 hora em doses de 300 mg ou menos. No entanto, verificou -se que os alimentos atrasam substancialmente a absorção da pregabalina e reduzem significativamente os níveis de pico sem afetar a biodisponibilidade do medicamento; Valores de TMAX para pregabalina de 0,6 horas em um estado de jejum e 3,2 horas em um estado alimentado (diferença de 5 vezes), e o CMAX é reduzido em 25 a 31% em um estado alimentado versus jejum. Em contraste com a pregabalina, os alimentos não afetam significativamente o TMAX da gabapentina e aumenta o cmax da gabapentina em aproximadamente 10%. A formulação Tmax da liberação instantânea (IR) de gabapentina enacarbil (como gabapentina ativa) é de cerca de 2,1 a 2,6 horas em todas as doses (350-2.800 mg) com administração única e 1,6 a 1,9 horas em todas as doses (350-2.100 mg ) com administração repetida. Por outro lado, o TMAX da formulação de liberação prolongada (XR) de gabapentina Enacarbil é de cerca de 5,1 horas em uma dose única de 1.200 mg em um estado de jejum e 8,4 horas em uma dose única de 1.200 mg em estado de alimentação. O TMAX do fenão não foi relatado, mas o início da ação e os efeitos de pico foi descrito como ocorrendo de 2 a 4 horas e 5 a 6 horas, respectivamente, após a ingestão oral em usuários recreativos que tomam doses altas (1-3 g) .
DistributionGabapentina, pregabalina e fenão atravessam a barreira hematoencefálica e entram no sistema nervoso central. No entanto, devido à sua baixa lipofilicidade, os gabapentinóides requerem transporte ativo através da barreira hematoencefálica. O LAT1 é altamente expresso na barreira sanguínea -alvo e transporta os gabapentinóides que se ligam a ele no cérebro. Assim como a absorção intestinal da gabapentina mediada por LAT1, o transporte de gabapentina através da barreira sanguínea -hidrográfica por LAT1 é saturável. A gabapentina não se liga a outros transportadores de drogas, como a glicoproteína P (ABCB1) ou OCTN2 (SLC22A5).
Gabapentina e pregabalina não estão significativamente ligadas às proteínas plasmáticas (<1%). O baclofeno analógico do fenão mostra baixa ligação de proteínas plasmáticas de 30%.
MetabolismGabapentina, pregabalina e fenão passam por pouco ou nenhum metabolismo. Por outro lado, a gabapentina Enacarbil, que atua como um pró -fármaco de gabapentina, deve sofrer hidrólise enzimática para se tornar ativa. Isso é feito por esterases não específicas no intestino e em menor grau no fígado.
EliminationGabapentina, pregabalina e fenão são todos eliminados renalmente na urina. Todos eles têm meias-vidas relativamente curtas de eliminação, com valores relatados de 5,0 a 7,0 horas, 6,3 horas e 5,3 horas, respectivamente. Da mesma forma, a meia-vida terminal da gabapentina Enacarbil IR (como gabapentina ativa) é curta em aproximadamente 4,5 a 6,5 horas. Verificou-se que a meia-vida de eliminação da gabapentina é estendida com doses crescentes; Em uma série de estudos, foram 5,4 horas para 200 mg, 6,7 horas para 400 mg, 7,3 horas por 800 mg, 9,3 horas para 1.200 mg e 8,3 horas por 1.400 mg, todas fornecidas em doses únicas. Devido à sua meia-vida de eliminação curta, a gabapentina deve ser administrada de 3 a 4 vezes por dia para manter os níveis terapêuticos. Da mesma forma, a pregabalina recebeu 2 a 3 vezes por dia em estudos clínicos. O Phenibut, também, é tomado 3 vezes por dia. Por outro lado, a Gabapentin Enacarbil é tomada duas vezes por dia e a Gabapentin XR (Nome da marca Gralise) é tomada uma vez por dia.
Química

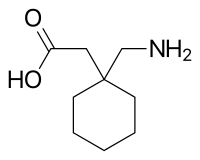
Os gabapentinóides são derivados de GABA em três substitutos do GABA; Portanto, eles são análogos do GABA, bem como γ-aminoácidos. Especificamente, a pregabalina é (s)-(+)-3-isobutil-gaba, o fenão é 3-fenil-gaba e a gabapentina é um derivado de GABA com um anel de ciclo-hexano na posição 3 (ou, um pouco nomeado, 3- ciclohexil-gaba). Os gabapentinóides também se assemelham aos α-aminoácidos L-leucina e à L-isoleucina, e isso pode ser de maior relevância em relação à sua farmacodinâmica do que sua semelhança estrutural com GABA.
História
Gabapentina, sob o nome da marca Neurontin, foi aprovada pela primeira vez em maio de 1993 para o tratamento da epilepsia no Reino Unido e foi comercializado nos Estados Unidos em 1994. Posteriormente, a gabapentina foi aprovada nos Estados Unidos para o tratamento da neuralgia póstética em Maio de 2002. Uma versão genérica da Gabapentin tornou-se disponível nos Estados Unidos em 2004. Uma formulação de Gabapentina de liberação prolongada para administração uma vez ao dia, sob a marca Gralise, foi aprovada nos Estados Unidos para o tratamento neuralgia posterpética em janeiro 2011.
A pregabalina, sob o nome da marca Lyrica, foi aprovada na Europa em 2004 e foi introduzida nos Estados Unidos em setembro de 2005 para o tratamento da epilepsia, neuralgia pós -pó e dor neuropática associada à neuropatia diabética. Foi posteriormente aprovado para o tratamento da fibromialgia nos Estados Unidos em junho de 2007. A pregabalina também foi aprovada para o tratamento de transtorno de ansiedade generalizada na Europa em 2005, embora não tenha sido aprovada para essa indicação nos Estados Unidos.
Gabapentin Enacarbil, sob o nome da marca Horizant, foi introduzido nos Estados Unidos para o tratamento da síndrome das pernas inquietas em abril de 2011 e foi aprovado para o tratamento da neuralgia pós -espética em junho de 2012.
O Phenibut, comercializado sob os nomes de marcas Anvifen, Fenibut e Noofen, foi introduzido na Rússia na década de 1960 para o tratamento da ansiedade, insônia e uma variedade de outras condições. Não foi descoberto atuar como gabapentinóide até 2015.
Mirogabalin, sob o nome da marca Tarlige, foi aprovado para o tratamento da dor neuropática e da neuralgia pós -coletiva no Japão em janeiro de 2019.
Sociedade e cultura
Uso recreativo
Os gabapentinóides produzem euforia em doses altas, com efeitos semelhantes aos depressores do sistema nervoso central GABAérgico, como álcool, ácido γ-hidroxibutírico (GHB) e benzodiazepínicos e são usados como drogas recreativas (com doses clínicas típicas de 3 a 20 vezes). O potencial geral de abuso é considerado baixo e notavelmente menor do que o de outras drogas, como álcool, benzodiazepínicos, opióides, psicoestimulantes e outras drogas ilícitas. De qualquer forma, devido ao seu potencial recreativo, a pregabalina é uma substância controlada pelo Anexo V nos Estados Unidos. Em abril de 2019, o Reino Unido agendou a Gabapentina e a Pregabalina como medicamentos de classe C sob a Lei de Uso de Uso de Drogas de 1971 e como Anexo 3 sob o uso indevido dos regulamentos de drogas 2001. No entanto, não é uma substância controlada no Canadá, ou na Austrália e Os outros gabapentinóides, incluindo o fenão, também não são substâncias controladas. Como tal, eles são principalmente intoxicantes legais.
É relatado que a tolerância aos gabapentinóides se desenvolve muito rapidamente com o uso repetido, embora também se dissipe rapidamente após a descontinuação e os sintomas de abstinência, como insônia, náusea, dor de cabeça e diarréia. Sintomas de abstinência mais graves, como ansiedade grave de recuperação, foram relatados com fenão. Devido à rápida tolerância aos gabapentinóides, os usuários geralmente aumentam suas doses, enquanto outros usuários podem espancar suas doses e usar com moderação para evitar tolerância.






